骨组织稳态是通过成骨细胞形成骨和破骨细胞吸收骨之间的平衡来维持的。然而,随着年龄的增长,成骨细胞功能下降,骨重塑失衡,骨量和密度下降,骨质疏松症发生,影响全球2亿人。激活成骨细胞和促进骨分化的分子被认为是发现骨质疏松症药物的种子。
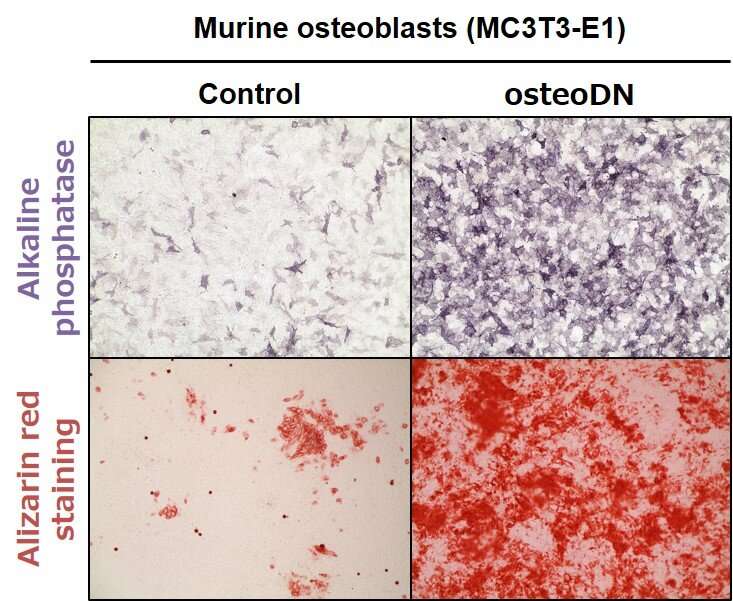
由助理教授Tomohide Takaya领导的研究小组此前发现了一种诱导肌肉分化的寡核苷酸(ODN)。研究组认为可能存在促进骨分化的ODN,并进行了这项研究。结果,该研究小组成功识别了一个18碱基的成骨ODN (osteoDN), iSN40,它促进小鼠成骨细胞从乳酸菌基因组序列衍生的44种ODN中分化。研究证实iSN40具有诱导骨分化和钙沉积骨细胞成熟所需基因表达的作用。iSN40有望作为一种激活成骨细胞的ODN,应用于治疗骨质疏松症的核酸药物。
本研究旨在直接作用于成骨细胞,促进骨分化,发现治疗骨质疏松症有用的核酸药物种子。虽然许多人由于骨质疏松而有骨折的风险,但目前使用的治疗药物是蛋白质/肽制剂,如抗体和激素(denosumab, romosozumab等),这些药物难以大量生产且价格昂贵。另一方面,核酸的合成成本很低。因此,Takaya助理教授希望提出核酸药物治疗骨质疏松症的可能性,因为核酸易于制造和储存,为下一代药物提供了潜在的纳米分子。
研究小组准备检查大量的DNA序列,并进行冗长的实验来寻找骨odn,当时不知道骨odn是否存在。他们准备进行一段漫长的实验,对许多DNA序列进行检测,但他们惊喜地发现,ODN是如此容易找到。有人可能会认为这可能只是运气,或者,助理教授高谷认为,这是我们还没有发现骨odn的事实。影响细胞命运的ODN序列,比如osteoDN,可能比我们之前认为的要多得多。
骨odn是一种短单链DNA,可以促进骨细胞的形成。这种成骨性骨dn有望成为治疗骨质疏松症的药物。下一步是在动物模型中展示骨形成的影响。最终,我们的目标是将其作为治疗骨质疏松症的药物应用于临床。
研究结果发表在《纳米材料》杂志上。